Anvisa autoriza dobrar número de voluntários em testes de vacina da Pfizer no Brasil
Com a medida, o número de participantes brasileiros passará de mil para 2 mil
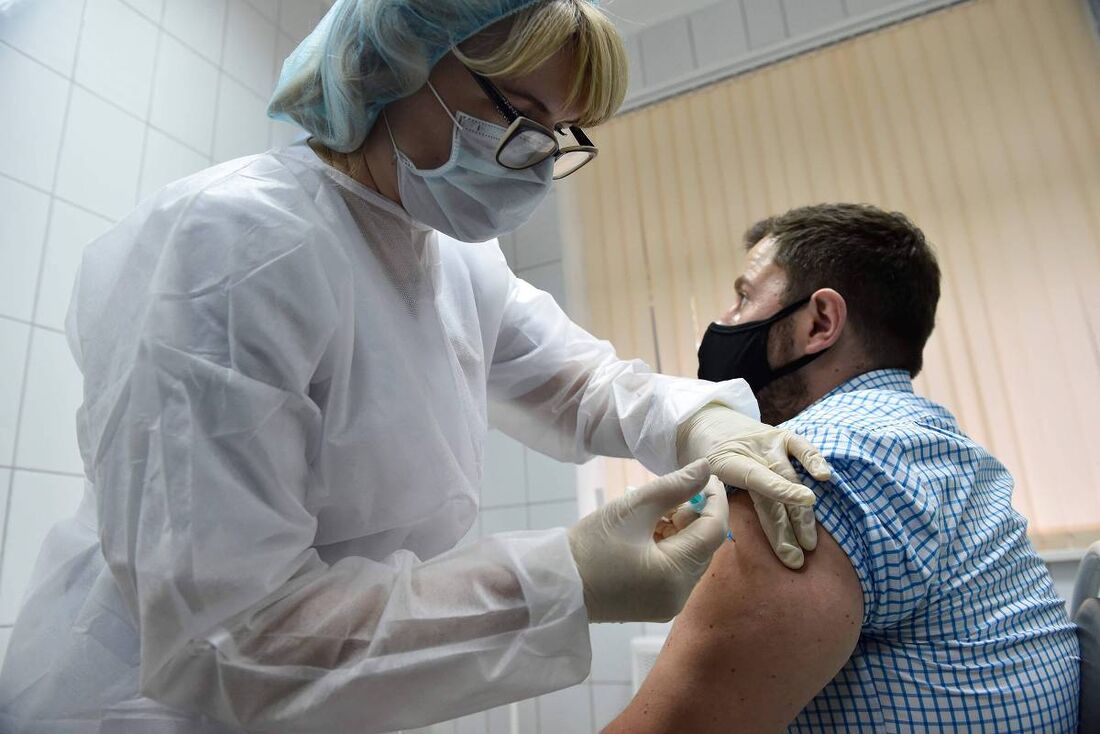
A Anvisa (Agência Nacional de Vigilância Sanitária) autorizou, nesta sexta-feira (18), a ampliação, no Brasil, dos testes clínicos de uma potencial vacina contra a Covid-19 em desenvolvimento pela farmacêutica Pfizer. Com a medida, o número de participantes brasileiros passará de 1.000 para 2.000.
Os testes são feitos em São Paulo e Bahia. Inicialmente, o estudo previa envolver até 29 mil voluntários em diferentes países, incluindo o Brasil. Agora, a previsão é que o total de participantes seja ampliado para 44 mil, de acordo com a empresa.
Além da ampliação no número de voluntários, a agência deu aval também para uma mudança na faixa etária dos participantes, cuja idade mínima passa de 18 anos para 16 anos.
A mudança ocorre após solicitação do laboratório, que conduz testes em conjunto com a empresa alemã de biotecnologia BioNTech. Além da possível vacina da Pfizer, o Brasil tem outros três estudos clínicos em andamento de potenciais imunizantes contra a Covid.
Leia também
• Brasil pede mais tempo para decidir se entra em aliança internacional por vacina
• Brasil terá maior fábrica de vacinas da América Latina
• Cobertura vacinal na pandemia está abaixo de 60%
O primeiro a obter aval para testes foi a vacina em desenvolvimento pela Universidade de Oxford com a farmacêutica AstraZeneca, o que ocorreu ainda em junho. Em seguida, tiveram autorização para estudos a empresa chinesa Sinovac, que conduz pesquisas em parceria com o Instituto Butantan, a empresa norte-americana Pfizer e a Janssen, braço farmacêutico da Johnson & Johnson. Essa não é a primeira mudança em testes clínicos de vacinas.
Na terça (15), a agência autorizou a ampliação do número de voluntários que devem fazer parte, no Brasil, de estudos da vacina em desenvolvimento pela Universidade de Oxford em parceria com a farmacêutica AstraZeneca.
Com isso, o total de participantes no país deve passar de 5 mil para 10 mil.
Além de permitir que seja ampliado o número de participantes, a agência também autorizou uma mudança na faixa etária de testes da vacina, que passa a incluir participantes maiores de 69 anos.

