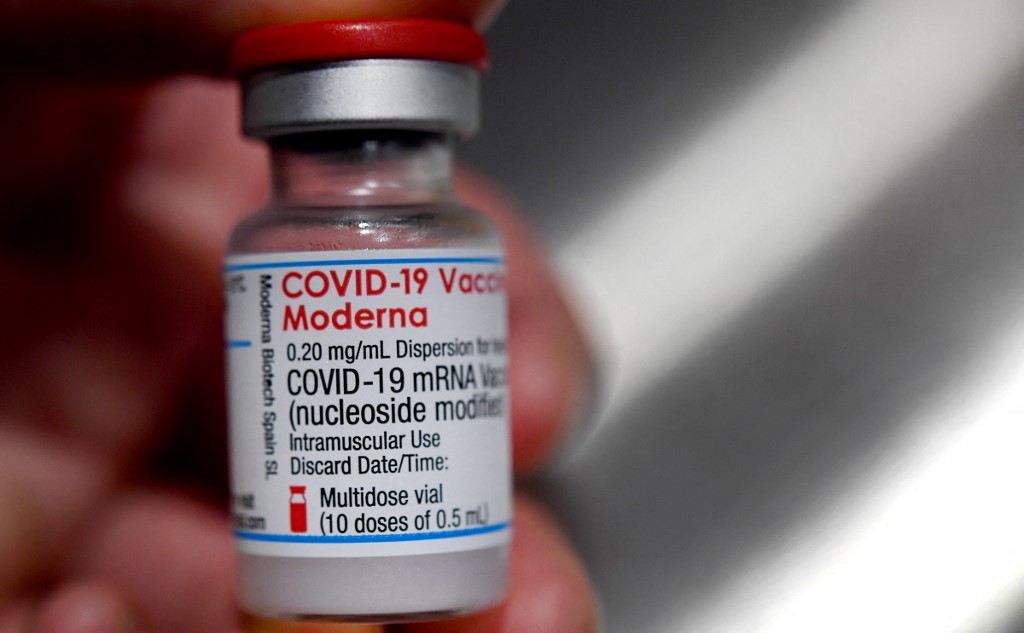
Aprovação de vacina da Moderna para adolescentes é adiada nos EUA
A avaliação para determinar a recomendação ou não da vacina da Moderna para jovens de 12 a 17 anos pode durar até janeiro de 2022, antecipou a companhia
A empresa americana de biotecnologia Moderna anunciou neste domingo (31) que as autoridades atrasaram a autorização de sua vacina contra a Covid-19 para adolescentes, a fim de ganhar mais tempo para avaliar melhor o risco potencial de miocardite ou inflamação cardíaca.
A Administração de Medicamentos e Alimentos (FDA) dos Estados Unidos "informou à Moderna que a agência requer tempo adicional para avaliar as recentes análises internacionais do risco de miocardite após a vacinação", explicou a empresa em um comunicado.
Leia também
• Prefeitura demite três funcionários que se recusaram a tomar vacina contra Covid
• Fiocruz: passaporte de vacina é indicado para ambiente de trabalho
• EUA autoriza vacina anticovid da Pfizer para crianças de 5 a 11 anos
A avaliação para determinar a recomendação ou não da vacina da Moderna para jovens de 12 a 17 anos pode durar até janeiro de 2022, antecipou a companhia.
A miocardite e um risco associado, a pericardite (inflamação ao redor do coração), foram previamente associados às vacinas anticovid da Pfizer e da Moderna, particularmente entre adolescentes e homens jovens.
No entanto, o risco é muito maior após a infecção pela Covid-19, de acordo com um estudo publicado em agosto pelos Centros de Controle e Prevenção de Doenças dos Estados Unidos (CDC).
O CDC descobriu que "a miocardite após a vacinação com vacinas de mRNA foi incomum e geralmente leve", ressaltou a Moderna.
Outra vacina de mRNA, a da Pfizer-BioNTech, recebeu liberação dos EUA na sexta-feira para crianças de 5 a 11 anos, em doses menores do que para adultos.