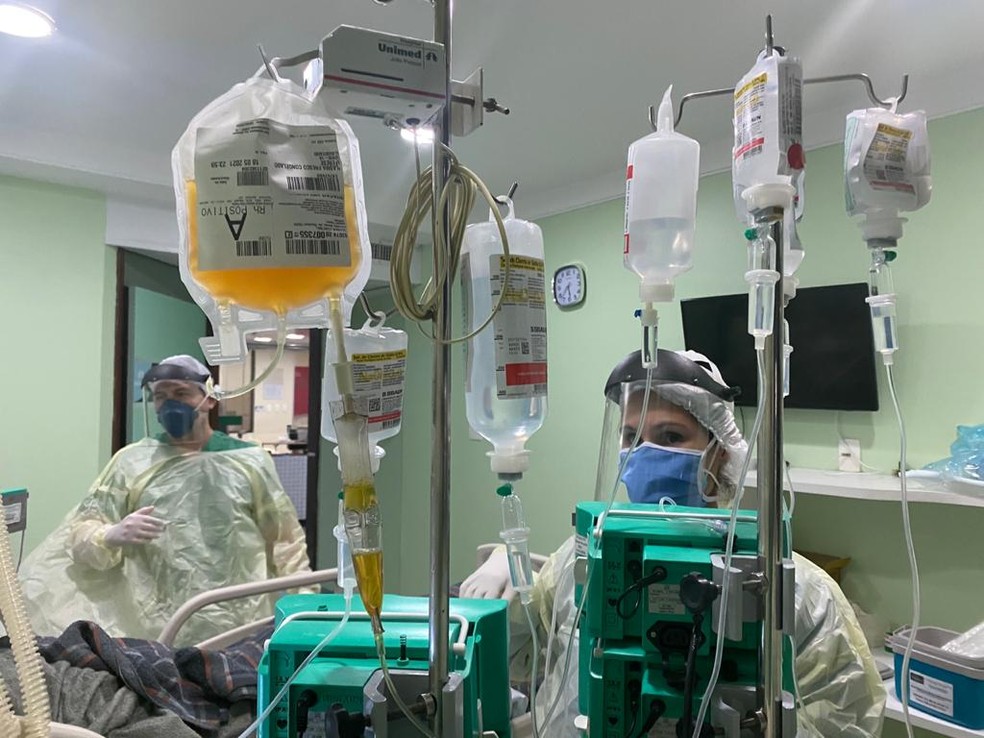
EUA suspende ensaio de tratamento com plasma para pacientes com a Covid-19
Resultados intermediários não mostraram benefícios com o tratamento
Os Institutos Nacionais dos Estados Unidos anunciaram, nesta terça-feira (2), a suspensão dos ensaios clínicos sobre um tratamento com plasma para pacientes com Covid-19 porque seus resultados intermediários não mostraram benefícios. Os testes desse procedimento, que envolve a transfusão de plasma de pessoas curadas da doença, começaram em agosto.
Pouco mais de 500 pessoas participaram do estudo após comparecer ao pronto-socorro de um hospital com sintomas leves ou moderados da Covid-19, que não necessitaram de internação.
Os escolhidos também apresentavam fatores de risco como obesidade, hipertensão, diabetes ou doenças cardíacas. Alguns receberam o plasma de curados da Covid-19, enquanto outros receberam um placebo.
Os pesquisadores, então, registraram o número de pessoas que necessitaram de cuidados de emergência adicionais ou morreram nos 15 dias seguintes.
Um comitê que avaliou os dados determinou que "embora o plasma convalescente não tenha causado nenhum dano, é improvável que tenha beneficiado o grupo de pacientes estudados", disse o Instituto de Saúde dos Estados Unidos (NIH) em um comunicado.
O chamado plasma convalescente é a parte líquida do sangue de um paciente curado que concentra os anticorpos produzidos para enfrentar o vírus após a infecção.
Leia também
• Câmara aprova texto-base de projeto que autoriza compra de vacinas por empresas privadas
• Paulo Câmara visita fábrica da Sputnik V no Brasil para negociar compra de vacinas
• Covax entregará 237 milhões de doses de vacinas a 142 países até maio
No final de outubro, um estudo realizado na Índia e publicado na revista médica BMJ concluiu que esse tratamento tinha uma "eficácia limitada”. De acordo com os cientistas, ele falhou em reduzir a mortalidade ou prevenir o agravamento das condições em pacientes com sintomas moderados.
Mais de 100 mil pessoas receberam esse tratamento nos Estados Unidos desde o início da pandemia e muitos mais no resto do mundo, de acordo com o NIH.
No final de agosto, e a pedido do então presidente Donald Trump, a agência de medicamentos dos Estados Unidos (FDA) autorizou com urgência o tratamento com plasma.
O então diretor da FDA, Stephen Hahn, admitiu, posteriormente, em uma coletiva de imprensa com Trump, que ele estava errado ao citar números que superestimaram os benefícios do tratamento.
Recentemente, a FDA restringiu sua autorização de emergência apenas para plasma com alta concentração de anticorpos e para pacientes hospitalizados com graus pouco avançados da doença ou com baixa capacidade de gerar anticorpos.